I. 背景紹介:
近年、マイクロ波支援合成法とフロー合成法の導入により、固相合成の効率と収率はさらに向上しました。しかしながら、これらの技術は一般的に高価で高度に特殊化された装置を必要とするため、日常的な研究室への普及は限定的です。さらに、Fmoc固相合成で広く使用されている活性化試薬であるHATUは、熱安定性が低く、安全性に懸念があります。
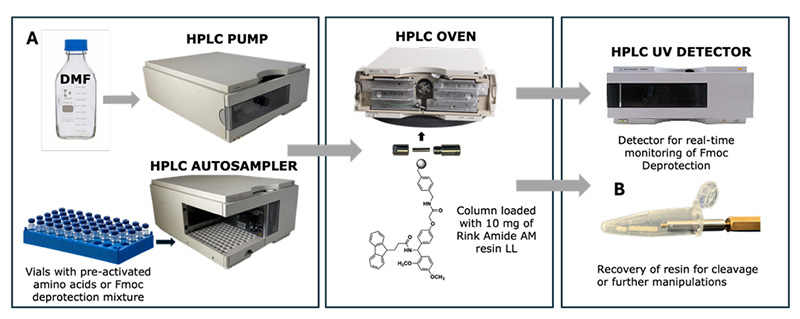
こうした状況を踏まえ、スイス、ジュネーブ大学のNicolas Winssinger氏率いる研究チームは、汎用液体クロマトグラフィーシステムをフローケミストリー技術向けに改造することで、高性能液体クロマトグラフィー(HPLC)からペプチド合成装置への転換を実現しました。
II. 液相法:
HPLCは、一般的に使用されている分離分析技術です。サンプルはクロマトグラフィーカラムを用いて成分に分離され、サンプルの純度が判定されます。本研究チームは、10mgの樹脂を充填したガードカラムプレカラムをマイクロフローリアクターとして革新的に使用し、内部に2μmの溶融塩を設けることで樹脂の損失を防止しました。同時に、DAD検出器(Fmoc脱保護副産物の検出)を用いて合成結果のリアルタイムフィードバックを提供しました。
このスキームでは、活性化システムとしてTBEC(1-tert-ブチル-3-エチルカルボジイミド)/オキシマ(2-オキシムシアノ酢酸エチル)を使用することで、追加のアルカリ添加や活性化前ステップが不要になり、プロセスが簡素化され、より安全で環境に優しいものとなっています。
上記の装置と活性化システムに基づき、合成条件を探索するために、フェニルアラニン五量体をモデルとして、改良したHPLCシステムで条件を最適化しました。実験結果から、最適化された条件で目的のペンタペプチドを合成し、粗生成物の純度は93%以上、単一ステップの純度は99%以上を達成したことが示されました。
具体的な方法は以下の通りです。
| 機器モデル |
アジレント 1260 インフィニティ |
| 自動サンプラーの容量 |
100μL |
カラム温度 |
80℃ |
| クロマトグラフィーカラム |
C18シリカゲルカラム / Hypersil Gold C18クロマトグラフィーカラム |
保護柱 |
樹脂充填(20 x 2 mm) |
| 検出器 |
DAD検出器 |
検出波長 |
360 nm |
| 流量 |
1.0 mL/分 |
移動相 |
移動相A: 活性エステル溶液 |
| 洗浄工程 |
時/分 |
0 |
0.1 |
1.5 |
2.0 |
| 移動相A |
100 |
100 |
100 |
100 |
III. 操作手順:
合成プロセス全体には次の段階が含まれます。
1. 樹脂の計量と充填:樹脂(Rink Amide樹脂など)を10mg計量し、空の保護カラムに充填し、密封して固定します。
2. 樹脂の膨潤:樹脂を充填した保護カラムをジクロロメタンに浸し、3〜5分間膨潤させます。
3. 取り付け:カラムオーブンの温度を80℃に設定し、保護カラムを対応するホルダーに取り付けます。
4.試薬溶液の調製:
サンプル溶液:0.6 M Fmocアミノ酸、TBEC、およびOxyma NMP溶液を調製し、等量で混合して0.2 M溶液を得ます。
脱保護溶液:20%ピペリジンをDMFに加え、後で使用するためにオートサンプラーバイアルに移します。
5. 注入シーケンスのプログラミング:活性化アミノ酸誘導体溶液(カップリング用)と20%ピペリジンDMF溶液(脱保護用)を交互に注入するように装置を設定します。さらに、合成開始前に脱保護を2回連続して行い、初期のFmoc基を完全に除去する必要があります。
6. 樹脂の溶解と脱保護:ガードカラムをジクロロメタンに浸して残留DMFを除去します。その後、樹脂を取り出し、TFA溶液(TFA/トリイソプロピルシラン TIS/H2O = 95:2.5:2.5)に3時間浸漬して、完全な解離と脱保護を達成します。システイン、メチオニンなどを含む特定の配列については、TFA/1,2-エチレンジチオール EDT/TIS/H2O = 90:5:2.5:2.5の混合溶解バッファーを使用できます。
7. 生成物の処理:樹脂を分離して粗ペプチドを沈殿させ、さらなる精製を行います。
IV. 影響要因:
ヒスチジンや一部の特殊アミノ酸などのラセミアミノ酸の場合、事前活性化時間はカップリング効率に大きな影響を与えます。 研究チームは20種類のペプチドの合成において、調製したばかりの活性エステルと24時間事前活性化したもののカップリング効率を比較したところ、Fmoc-Arg(pbf)-OHとFmoc-His(Trt)-OHは活性化時間が長くなるとカップリング効率が比較的低くなることがわかりました。
事前活性化時間がカップリング効率に及ぼす影響をさらに調べるため、Fmoc-Arg(pbf)-OHを原料として、事前活性化時間をそれぞれ15分と24時間に設定し、FRFトリペプチドを合成しました。 その結果、24時間の事前活性化後にはカップリング効率が大幅に低下することが示されました。これは、活性化後にFmoc-Arg(pbf)-OHが分子内環化を起こし、反応性が低下するためです。繰り返しの実験により、理想的な活性化溶液は調製後 4 時間以内に使用する必要があることが確認されました。
V. 示差異性化:
ペプチド合成中の異性化は、立体化学的純度に影響を与え、生物学的活性を変化させる可能性がある。これらの合成条件下でのラセミ化の程度を評価するため、研究チームは液相合成法を用いて、プロリン、システイン、セリンといった容易にラセミ化しやすいアミノ酸を調べたが、いずれのアミノ酸においてもラセミ化は観察されなかった。さらに、TBEC/Oxyma系とHATU/DIPEA系のカップリング効果を比較するため、研究チームは反応に活性化したばかりのHis(Trt)を用いた。実験の結果、前者は3.6%のエピマー化を示したのに対し、後者は4.8%の異性化率を示した。
VI. 実用的な応用:
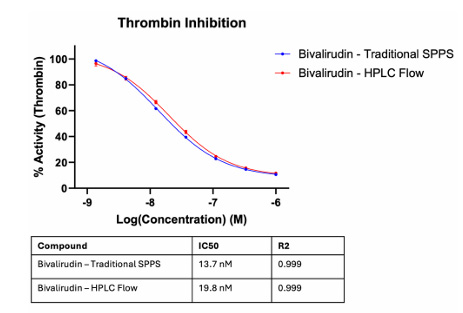
研究チームは、GLP-1(30アミノ酸)やビバリルジン(20アミノ酸)などのペプチドの合成に成功しました。10mgの樹脂を含む合成カラムを用いて合成したGLP-1は、収率52.1%でした。生理活性に関しては、HPLCで合成した粗ビバリルジンと従来のSPPS法で合成した純粋ビバリルジンは、いずれも同等の生理活性を示しました(下図参照)。
図5
VII. 利点と限界:
ペプチドの自動流体合成に適用される、すぐに利用できる HPLC システムには、次のような利点と欠点があります。
1. 利点:
- 標準 HPLC を多機能合成プラットフォームに変換します。
- より安全な TBEC/Oxyma 活性化システムを採用します。
- 高純度のペプチドを取得し、反応をリアルタイムで監視できます。
- 優れた立体選択性を示し、複雑な配列を持つポリペプチドを合成できます。
- 経済的であり、広く入手可能な HPLC 機器を使用し、機器コストを削減し、より多くの研究室に利益をもたらします。
- 高い柔軟性を備え、ペプチド/オリゴヌクレオチドの合成に使用できます。また、カラムを交換することで合成モードと精製モードを切り替えることも可能です。
2. 制限事項:
- 特定の複雑な配列を合成することはできません。
- 反応速度はアミノ酸やペプチド鎖によって異なるため、さらなる最適化が必要です。
- 合成量が少なく、マイクログラムからミリグラムレベルでの合成にのみ適しています。
VIII. 全体的な結論:
本研究は、従来のHPLCシステムを用いて反応と検出を同時に行うことができる、簡便で安全かつ経済的なペプチド合成プラットフォームを提供する。このアプローチは、生成物の立体化学的な完全性を維持するだけでなく、複雑で生物学的に活性な配列フラグメントの合成も可能にし、より多くの研究室におけるフロー合成技術の普及に貢献する。
Highfine Biotechについて:
蘇州ハイファインバイオテック株式会社(証券コード:301393.SZ)は、2003年に設立され、蘇州ハイテク産業開発区に本社を置く、国家ハイテク企業です。世界中の医薬品研究開発・製造企業に特殊原料を提供しています。製品は主にペプチド、ヌクレオチド、医薬品合成に使用され、特殊アミド結合形成用縮合剤、保護剤、リンカー、抗体薬物複合体用タンパク質架橋剤、分子ビルディングブロック、リポソーム、リン試薬など、幅広い製品を取り扱っています。現在、1500種類以上の製品を開発・製造しています。
22年間のたゆまぬ努力と蓄積を経て、ハイファインバイオテックは世界的なペプチド合成試薬分野における専門知識を継続的に深化させ、現在では幅広いカスタマイズ製品と大規模生産における大きな優位性を備えたリーディングカンパニーへと成長し、様々な顧客の具体的なニーズに対応しています。当社の製品にご関心をお持ちのお客様は、詳細情報や協力の可能性についてお気軽にお問い合わせください。
参考文献:
[1] Romanens, P.; Barluenga, MD; Winssinger, N., et al. Peptides on Tap: 標準HPLCによる自動フロー合成 [J]. ChemRxiv. 2025.