3/26/2026
生命過程において重要な役割を果たすペプチドは、効率的かつ精密な合成法が必要とされるため、化学合成の分野で常に研究のホットスポットとなってきた。従来のペプチド合成法では、通常、カルボキシル基を活性化して活性エステルまたはその他の反応性物質に変換し、それを別の分子のアミノ基と結合させる。この方法は広く用いられているが、通常はC→N合成に限定され、システインのような敏感なアミノ酸を扱う場合、ラセミ化などの副反応が起こりやすい。このボトルネックに対処するため、J.-M. Campagneのチームは異なるアプローチを取り、「逆活性化」戦略、すなわちアミノ基を活性化する新しいペプチド合成法を開発した。
生命過程において重要な役割を果たすペプチドは、効率的かつ精密な合成法が必要とされるため、化学合成の分野で常に研究のホットスポットとなってきた。従来のペプチド合成法では、通常、カルボキシル基を活性化して活性エステルまたはその他の反応性物質に変換し、それを別の分子のアミノ基と結合させる。この方法は広く用いられているが、通常はC→N合成に限定され、システインのような敏感なアミノ酸を扱う場合、ラセミ化などの副反応が起こりやすい。このボトルネックに対処するため、J.-M. Campagneのチームは異なるアプローチを取り、「逆活性化」戦略、すなわちアミノ基を活性化する新しいペプチド合成法を開発した。
I. 「活性化カルボン酸」から「活性化アミノ酸」への逆算思考
従来の方法の核心はカルボキシル基の活性化にあるが、J.-M.カンパーニュの研究チームは、活性化部位をアミノ基に巧みに移した。彼らは、安価で入手しやすいN,N'-カルボニルジイミダゾール(CDI)をトリエチルアミンの存在下でα-アミノ酸エステルと反応させ、安定なN-イミダゾリウムカルボキシルアミノ酸エステル中間体を生成・単離した(図1)。この中間体は「活性化アミノ基」に相当し、数ヶ月間安定して保存できる。
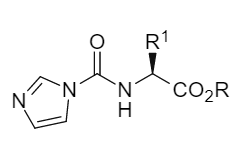
図1 N-イミダゾリルアミノ酸エステルの一般式
2 )の存在下でN保護アミノ酸と直接反応し、52~90%の収率でジペプチドが得られる。この方法は、Fmoc、Boc、Cbzなどの一般的に使用されるカルバメート保護基と互換性があり、反応基質が容易にラセミ化するシステインを含む場合でもラセミ化は観察されなかった。しかし、研究によると、従来のペプチド合成溶媒であるDMFはこのシステムには適していない。
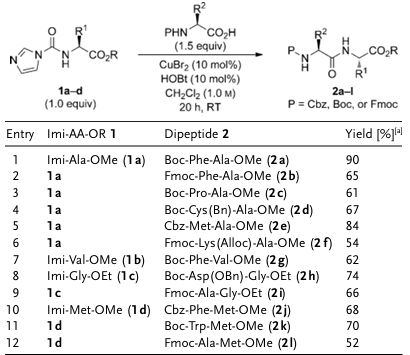
図2.「活性化アミノ基」を介したジペプチドの合成
この合成戦略の可能性をさらに検証するため、研究チームはN→C方向からのテトラペプチド合成を試み、最終的にラセミ体生成物を一切検出することなく、目的生成物を25%の収率で得た。この発見は、逆ペプチド合成におけるこの方法の大きな可能性を示しており、複雑なペプチド医薬品や生理活性分子を合成するための信頼性の高い新たな経路を提供するものである。
II. ワンポット合成:高効率、原子効率、および良好な立体選択性。
カンパーニュ氏(J.-M.)の研究チームは、これまでの研究成果を基に合成戦略をさらに最適化し、ジペプチドを合成するためのワンポット法を開発した。この方法は、穏やかな中性条件下で実施でき、アルカリ剤を必要とせず、N-イミダゾリウムカルボキシルアミノ酸エステル中間体をその場で生成する。分離精製の必要がないため、これらの中間体は市販の保護アミノ酸と直接反応させることができ、操作プロセスを大幅に簡素化できる。
実験結果から、このワンポット法は様々なジペプチド誘導体を効率的に合成でき、収率は最大87%に達し、様々なN-カルバメート保護基と適合し、優れた立体化学的安定性を示すことが明らかになった。さらに、プロリンは第二級アミン構造を持つため、アミノ活性化によるジペプチド合成が困難であることが分かった。
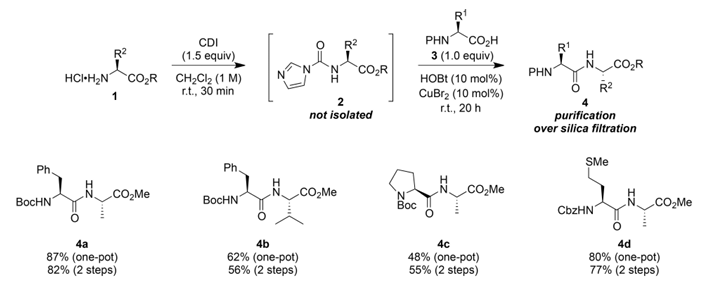
図3 ジペプチドのワンポット合成
2段階法とは異なり、ワンポット法では、系内で生成されたイミダゾールを「アミノ基の活性化」の際に塩基として利用し、イミダゾール塩を形成するため、追加の塩基は不要となる。また、この研究では、カップリング反応中に余分な塩基を加えると、活性化されたアミノ基とカルボン酸との間のアミド結合反応が阻害されることも明らかになった。
III.マイクロ波支援反応:反応速度を速め、サイクル時間を短縮する
合成効率を向上させるため、J.-M.カンパーニュの研究チームはさらにマイクロ波支援技術を導入し、「アミノ活性化」戦略への応用を模索した。
2段階合成法に基づき、マイクロ波照射を用いてアミドの結合反応を促進した(図4)。その結果、マイクロ波照射により反応速度が大幅に向上し、従来の20時間から1時間へと反応時間を短縮できることが示された。しかも、良好な収率を維持し、ラセミ化も観察されなかった。さらに、この方法を従来のアミドの合成にも適用したところ、期待通りの収率が得られた。
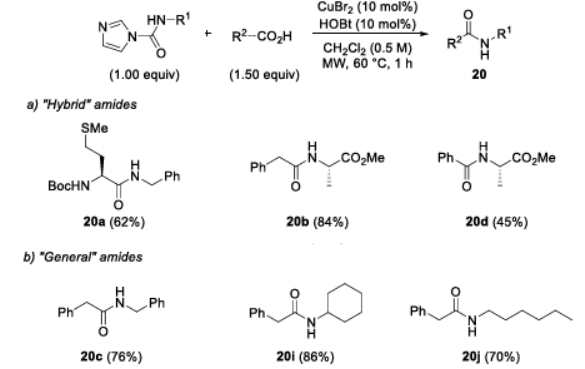
図4 マイクロ波を用いたペプチド合成
実験観察に基づき、研究チームは妥当な反応経路を提案した(図5):反応中に混合カルバミン酸無水物中間体が形成され、続いて分子内再配列と二酸化炭素の放出が起こり、最終的に目的のペプチド結合が生成される。
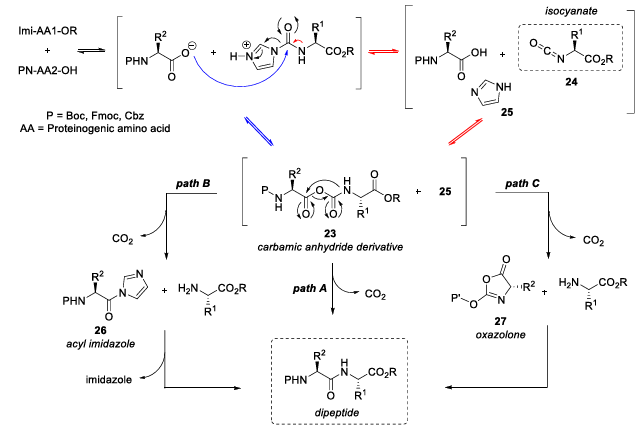
図5 反応機構
要約すると、J.-M. Campagneの研究チームが開発したCDIを介したα-アミノ酸エステル活性化戦略は、ペプチド結合形成のための穏やかで実用的かつ原子効率の良い新たな選択肢を提供する。この方法は、反応過程における敏感なアミノ酸のラセミ化問題を効果的に回避するだけでなく、困難なN→C方向のペプチド合成も成功裏に達成する。ペプチド医薬品開発への関心の高まりに伴い、この革新的な合成戦略は研究者のツールボックスに重要な追加となることが期待される。
会社概要:
蘇州浩凡生物科技有限公司(証券コード:301393.SZ)は、2003年に設立され、蘇州ハイテク区に本社を置く、世界中の製薬研究開発・製造企業に特殊原料を提供する国家級ハイテク企業です。同社の製品は主にペプチド、ヌクレオチド、医薬品の合成に使用され、特殊アミド結合用縮合剤、保護剤、連結剤、抗体薬物複合体用タンパク質架橋剤、分子ビルディングブロック、リポソーム、リン試薬など、幅広い製品を網羅しています。現在までに、累計1,500種類以上の製品を開発・製造しています。
20年以上にわたる弛まぬ努力と蓄積を経て、Haofan Biotechは世界のペプチド合成試薬分野における専門知識を継続的に培ってきました。現在では、幅広いカスタマイズ製品ラインナップと大規模生産における大きな強みを持つリーディングカンパニーへと成長し、多様なお客様のニーズにお応えできる体制を整えています。本製品にご興味をお持ちのお客様は、ぜひ当社までお問い合わせいただき、製品の詳細や協力関係の可能性についてご相談ください。
参考文献:
[1] 活性化α-アミノエステルを介した逆ペプチド合成。
DOI: 10.1002/anie.201402147
[2]シーケンシャルワンポット料理合成のジペプチドを通しての一時的な形成のCDI-N保護α-アミノエステル。
DOI: 10.1002/adsc.201700034
[3]アミン活性化:「逆」ジペプチド合成と活性化アミノ化合物によるアミド機能形成。
DOI: 10.1021/acs.joc.2c01288
ご興味のある関連商品をご紹介いたします。ご不明な点がございましたら、お気軽にお問い合わせください。
ペプチド合成試薬のお見積もりは下記のフォームにご記入ください。