2/10/2022
アミドは化学合成、特に実験室合成で頻繁に使用される縮合アシル化によるアミドの調製に広く使用されています。 カルボン酸とアミンの反応は、アミドを合成するための重要な方法です。この反応は平衡反応であり、反応物質の 1 つを過剰に使用するか、反応で生成した水を除去すると、平衡を生成物に向けてシフトするのに役立ちます。 。 この記事では、アミンによるいくつかのカルボン酸の縮合アシル化について説明します。
1.まず
アミドは化学合成でよく使用され、特に実験室での合成でよく使用される縮合アシル化によるアミドの調製に使用されます。カルボン酸とアミンの反応は、アミドを合成するための重要な方法です。この反応は平衡反応であり、反応物の1つを過剰に使用するか、反応で生成された水を除去することで平衡を変更できます。生成物に向かって。この記事では、さまざまなカルボン酸とアミンの縮合アシル化について説明します。
2. アミドの縮合による合成アシル化法。
2.1 混合無水物クロロギ酸法
主な用途は、カルボン酸をエチルクロロギ酸またはイソブチルエステルと反応させて混合無水物を形成し、次にアミンと反応させて対応するアミドを得ることである。この反応では、酸のA部位が妨害されていたり、電子吸引基を持っている場合、混合無水物段階で停止することがあります。しかし、加熱すると反応が促進される可能性があり、この反応は非置換アミドの合成にも使用できます。(図1)

図1
2.2 混合無水カルボニルジイミダゾール法
カルボニルジイミダゾール(CDI)をカルボン酸と反応させて、活性の高いアシルイミダゾールを得る。多くのアシルイミダゾールは一定の安定性を持ち、時には分離することができる。しかし、一般的に言えば、分離する必要はなく、反応溶液はアミンと直接反応して対応するアミドを調製する。カルボニルジイミダゾールとメチルトリフラートの反応によって得られるジメチル化トリフルオロメタンスルホネート(CBMIT)は、文献で報告されている。 )は、より優れた縮合性能を有する。(図2)

図2
2.3 混合無水物スルホニルクロリド法
カルボン酸とスルホニルクロリドはカルボン酸-スルホン酸混合無水物を形成し、アミンと反応して対応するアミドを与える[1]。一般的に使用されるスルホニルクロリドには、メタンスルホニルクロリド(MsCl)、p-トルエンスルホニルクロリド(TsCl)、p-ニトロベンゼンスルホニルクロリド(NaCl)などがある。p-ニトロベンゼンスルホニルクロリドは、その電子吸引特性により、酸と反応してより高い活性を生成する。混合酸無水物、一般的な第二級アミンおよび第三級アミン、さらには立体障害の大きいアミンでもスムーズに反応することができる。(画像3)

画像3
2.4 混合無水物 Boc無水物法
酸とBoc無水物およびアンモニアを反応させて得られた混合無水物を反応させることで、対応する第一級アミドが得られる。(図4)
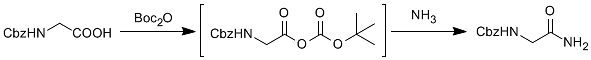
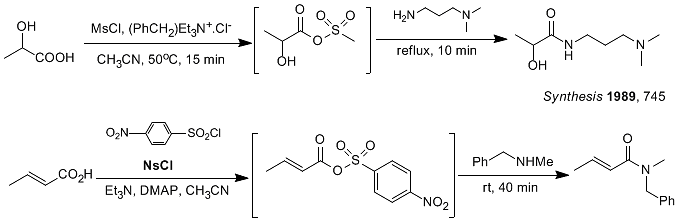
図4
2.5 カルボジイミド縮合剤 DCC 縮合法
一般的に、DCC と DMAP を併用します。DCC を使用する最大の欠点の 1 つは、反応のもう 1 つの生成物であるジシクロヘキシル尿素が、一般的な有機相では溶解度が小さいが、わずかに溶解することです。そのため、一般的に使用されている精製方法、再結晶、カラムクロマトグラフィーなどでは、ジシクロヘキシル尿素を完全に除去することは困難です。ジシクロヘキシル尿素のエーテルへの溶解度は他の溶媒に比べて比較的小さいため、通常は反応溶媒を蒸留し、エーテルを加えてジシクロヘキシル尿素の大部分をろ過する必要があります。その後、ジシクロヘキシル尿素をさらに処理します。(図 5)
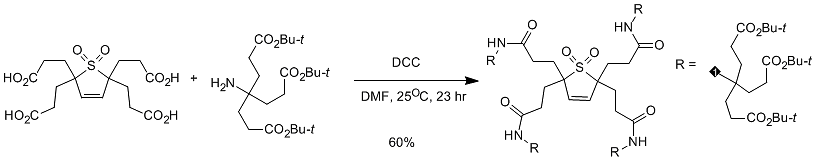
図5
2.6 カルボジイミド縮合剤 DIC 縮合法
DIC で生成されるジイソプロピル尿素は一般的な有機溶媒への溶解性が優れているため、コンビナトリアルケミストリーの固相合成でよく使用されます。(画像 6)
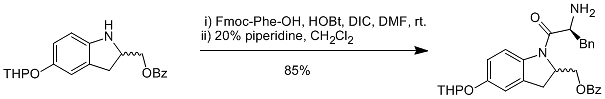
画像6
2.7 カルボジイミド縮合剤 EDCI 縮合法
現在、EDCI は医薬化学で最も多く使用されています。その主な特徴の 1 つは、反応後に生成される尿素が水溶性であり、簡単に洗い流せることです。通常、EDCI は HOBt と組み合わせて使用されます (注: この反応では HOBt が一般的に不可欠です。そうでない場合、縮合収率が低くなりすぎる可能性があります)。(図 7)
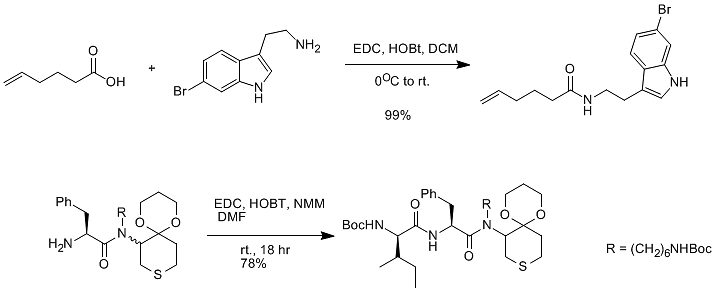
図7
2.8 カルベニウム塩の縮合剤法
現在一般的に使用されているのは、O-(7-アザベンゾトリアゾール-1-イル)-ビス(ジメチルアミノ)カルベニウムヘキサフルオロホスフェート(HATU)、O-(ベンゾトリアゾール-1- 塩基)-ビス(ジメチルアミノ)カルベニウムヘキサフルオロホスフェート(HBTU)、O-(5-クロロベンゾトリアゾール-1-イル)-ビス(ジメチルアミノ)カルベニウムヘキサフルオロホスフェート(HCTU)、O-(ベンゾトリアゾール-1-イル)-ビス(ジメチルアミノ)カルベニウムテトラフルオロボレート(TBTU)、O-(N-スクシンイミド)-ジ(ジメチルアミノ)カルベニウムテトラフルオロボレート(TSTU)、O-(N-エンド-5-ノルカンフェン-2,3-カルボジイミド)-ビス(ジメチルアミノ)カルボニウムテトラフルオロボレート(TNTU)などである(図 8)
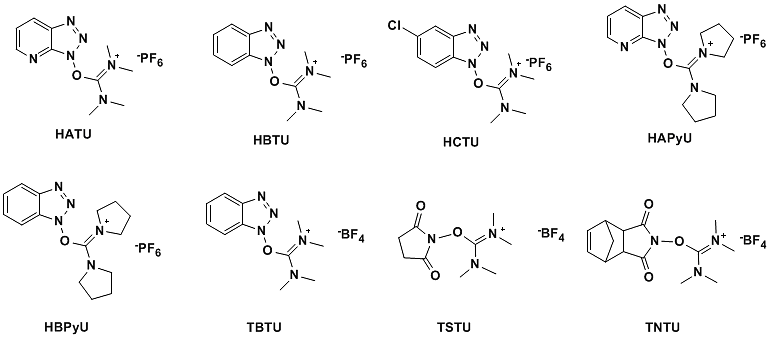
図8
HATU は最も活性の高いカルベニウム塩縮合剤であり、他の縮合剤がうまく機能しない場合によく使用されます。HBTU はほとんどの縮合反応に使用できますが、その低収率が大量生産での使用を制限する主な理由です。HCTU は活性が高く、工業生産で HATU を置き換えることができます。その高い活性は、より活性の高い Cl-HOBt 中間体によるものです。TSTU と TNTU は、水性溶媒中のアミド化反応に使用できます。HATU と HBTU のジメチルアミノ基をテトラヒドロピロリルに変更すると、活性の高い O-(7-アザベンゾトリアゾール-1-イル)-ジ(テトラヒドロピロリル) 炭素が得られます。オニウムヘキサフルオロリン酸 (HAPyU)、O-(ベンゾトリアゾール-1-イル)-ジ(テトラヒドロピロリル)カルベニウムヘキサフルオロリン酸 (HBPyU)。
カルベニウム塩縮合剤をアミド縮合に使用すると、主に分子内移動により対応する活性エステルが一段階で得られます。HATU の縮合反応を例に、その反応機構を説明します。(図 9)
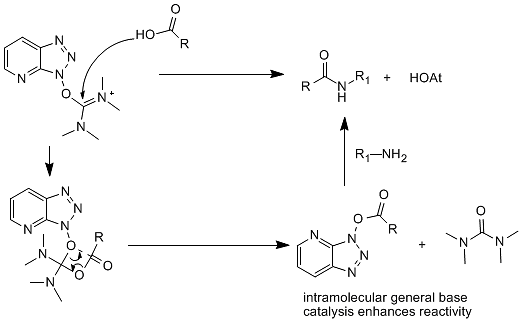
図9
2.9 ホスホニウムオニウム塩の縮合剤
最も古いものは、ヘキサメチルホスホルアミド (HMPA) の発がん性副産物であるベンゾトリアゾール-1-イルオキシ-トリス(ジメチルアミノ)ホスホニウムヘキサフルオロホスフェート (BOP) 試薬です。近年では、より活性が高く、発がん性副産物を生成しないベンゾトリアゾール-1-イルオキシ-トリス(テトラヒドロピロリル)ホスホニウムヘキサフルオロホスフェート (PyBOP) に置き換えられています。(図 10)
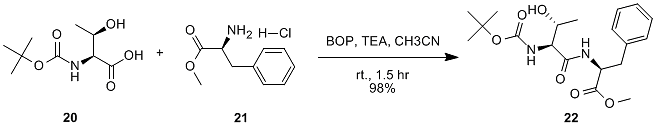
図10
PyBOP は比較的強力な縮合剤です。一般的に、他の縮合剤がうまく縮合しない場合に、PyBOP を使用するとより良い結果が得られます。たとえば、PyBOP はアミノ酸を塩化アンモニウムと縮合して対応するアミノアミドを得るために使用できます。(図 11)
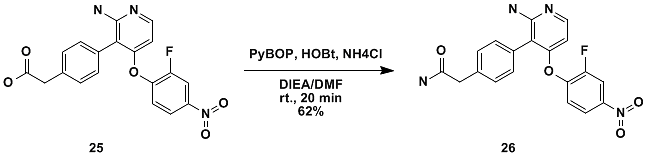
図11
2.10 有機リン縮合剤
DECP は、少数のポリペプチドの合成によく使用され、BOP-Cl は特にアミノ酸の合成に適しており、収率とラセミ化が良好です。ただし、アミンの反応性が低いとアシル化オキサゾリジンが得られることが多いという欠点があります。BOP-Cl の溶解性が低いため、反応時間が長くなり、4~5 日かかることもあります。反応溶媒として DMF がよく使用されます。(図 12)
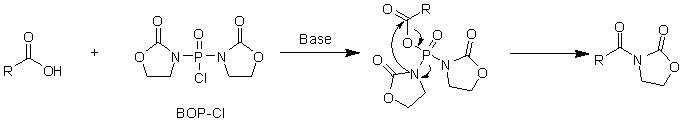
図12
DPP-Clを縮合剤として使用するとアミドを合成できます[2]。図13はDCCでは収率が15%に過ぎないのに対し、DPP-Clでは94%の収率を示しています。
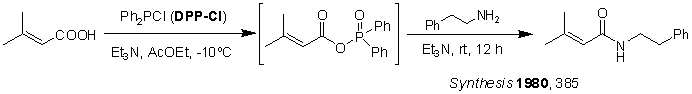
図13
2.11その他の縮合剤
トリフェニルホスフィン-ポリハロメタン[3]、トリフェニルホスフィン-ヘキサクロロアセトン[4]、トリフェニルホスフィン-NBS[5]などもアミドの縮合に使用できる。(図14)
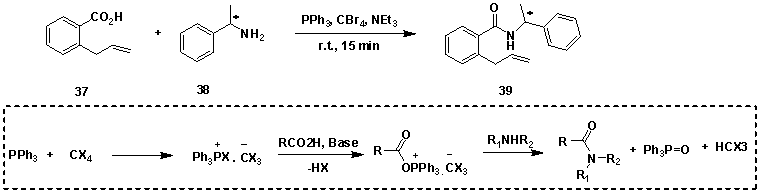
図14
DMTMMは縮合剤として使用され、アルコールまたは水中で反応を行うことができることが報告されています。(図15)
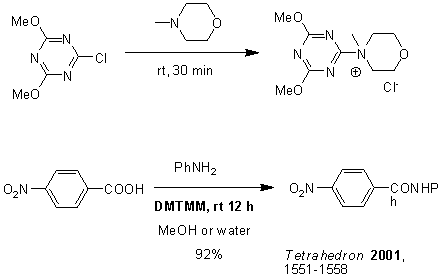
図15
トリフェニルホスフィン-ヘキサクロロアセトン(図16)、トリフェニルホスフィン-NBS(図17)もアミドの合成に使用できます。
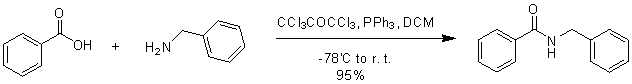
図16
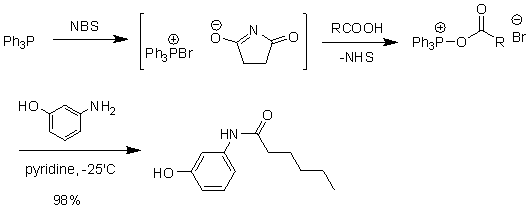
図17
参照:
[1] SJ Lau、JP Laussac、B Sarkar. Biochem J. 1989; 257(3): 745-750
[2] Böcker W、Dralle H、Hüsselmann H、Bay V、Brassow M. 1980; 385(2): 187-200。
[3] A Ignatious、J Rahul.1990;232(2):1105-1112.
[4] GBヴィルヌーヴ、THチャン1997;38:6489–6492。
[5] Higuchi H, Shimizu K, Ojima J, Sugiura K.1995; 36: 5359-5362.
ご興味のある関連商品をご紹介いたします。ご不明な点がございましたら、お気軽にお問い合わせください。
ペプチド合成試薬のお見積もりは下記のフォームにご記入ください。