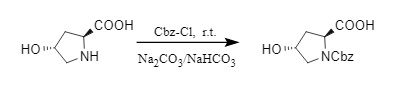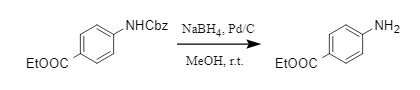1. はじめに
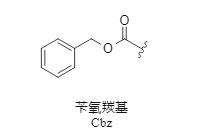
Cbzは最も一般的に用いられるアミノ保護基の一つです(1)。その利点は、導入と除去が容易なことです。さらに、Cbz保護基の導入により、保護された生成物は通常、結晶化しやすくなり、安定性が向上するため、結晶化による精製が容易になります。
(1)
2. 導入方法
1. アルカリ条件:
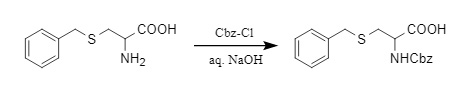
(1) Cbz保護基を導入する方法は数多くあります。最も一般的に用いられる方法は、アルカリ条件下でクロロギ酸ベンジル(Cbz-Cl)と反応させ、N-Cbz保護アミノ化合物(2)を生成することです。Cbz-Clに加えて、N-ベンジルスクシンイミジルカーボネート(Cbz-Osu)や4-ニトロフェニルベンジルカーボネート(Cbz-ONB)などの活性エステルも、ベンジルオキシカルボニル基を導入するための試薬として使用できます。
(2)
(2)Cbz-Clを用いてアルカリ条件下でCbzを導入する場合、pHは通常8~10に制御されます。pHが低すぎるとCbz-Clが分解し、pHが高すぎるとアミノ酸のラセミ化が起こる可能性があります。そのため、塩基は、このプロセスで生成されたHClを中和する酸結合剤として作用するだけでなく、大規模生産ではやや難しい反応系のpH安定性を維持する役割も果たします。Abellチームは、Na2CO3:NaHCO3=2:1の混合塩基緩衝系を開発しました。この系はpHを8~10の範囲に効果的に維持でき、さまざまなキラルアミノ酸のCbz保護に適しています(3)。
(3)
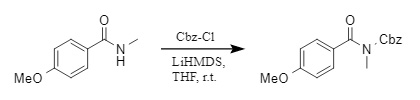
(3) さらに、Sureshbabuらの研究グループは、二級アミドの窒素原子にCbz保護基を導入する簡便な方法を開発しました(4)。塩基LiHMDS(リチウムビス(トリメチルシリル)アミド)の存在下で、二級アミドはCbz-Clと反応し、N-Cbz保護を達成することに成功しました。
(4)
2. 非アルカリ条件:
Cbz保護基は、非アルカリ条件下においてもN-Cbzを穏やかかつ効率的に保護するために用いることができる。
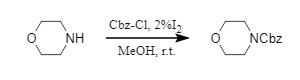
(1) Cbz-Cl/I2/MeOH:
Varalaらの研究チームは、Cbz保護基を効率的に導入するためのヨウ素触媒法を開発した。触媒量のヨウ素はルイス酸として作用し、構造と電子的性質が大きく異なるアミン化合物にCbz保護基を穏やかかつ効率的に導入する(5)。
(5)
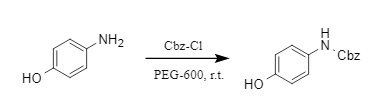
(2) Cbz-Cl/PEG-600:
黄海紅教授の研究チームは、効率的で環境に優しく、化学的に選択的なCbz保護基導入法(6)を開発しました。この方法では、環境に優しく毒性の低いPEG-600を反応媒体として使用します。脂肪族アミンおよび芳香族アミンはCbz-Clと反応し、対応するN-Cbz誘導体を高収率で得ることができます。
(6)
3. 除去方法
Cbz保護基の除去には様々な方法がありますが、最も一般的なのは接触水素化分解です。基質に他の敏感な基が含まれている場合は、酸性、アルカリ性、またはその他の条件下での選択的な脱保護が検討されます。
1. 接触水素化分解:
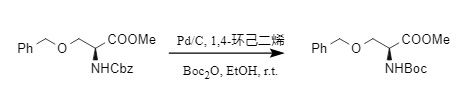
接触水素化分解には、接触水素化と移動水素化があり、どちらもCbzの除去に適しています。通常、水素源が十分な場合は二酸化炭素とトルエンが生成され、水素源が不十分な場合は副反応が起こり、N-ベンジル保護された三級アミンが生成されます。系内にBoc2Oも存在する場合、N-Cbz保護を1段階でN-Boc誘導体に変換することができ、ベンジルエーテルなどの還元されやすい官能基は影響を受けません(7)。
(7)
さらに、Pd-C/NaBH4/MeOHの組み合わせもCbzを除去する簡便な方法である(8)。この方法は、その場で水素を発生させることでCbzを迅速かつ簡便に除去することができ、多くの従来の保護基との適合性も良好である。
(8)
2. 酸性条件:
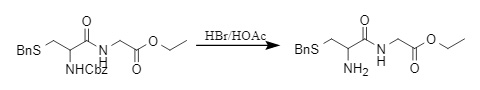
Cbz保護基は酸性条件下でも容易に除去できます。HBr/HOAcは一般的に用いられるCbz除去系です(9)。脱保護速度はHBr濃度の上昇とともに増加します。
(9)
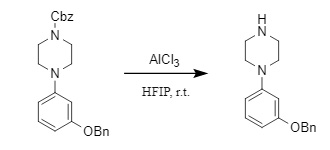
同様に、ルイス酸はN-Cbz保護の除去にも使用できます。AlCl3/HFIP(ヘキサフルオロイソプロパノール)系は、ニトロ基、二重結合、ベンジル基などの敏感な基が存在する場合でも、穏やかかつ安全にCbz保護を選択的に除去することができ、基質適用性も良好です(10)。
(10)
3. アルカリ条件:
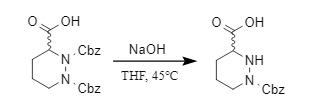
特定の条件下では、アルカリ条件でもCbz保護基の除去が可能です。例えば、N,N'-ビスCbz保護ジアジノ酸化合物では、アルカリ条件下で1つのCbz保護基を選択的に除去できます(11)。さらに、高濃度水酸化ナトリウム溶液中では、カナマイシンA中間体のN-3'位など、特定の位置にあるCbz保護基を選択的に除去できます。
(11)
4. その他の条件:
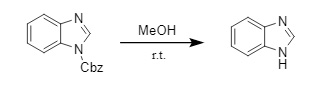
上記の脱保護法に加えて、特定の条件下でN-Cbz保護基を除去する方法は他にも数多く存在します。例えば、低級アルコール(メタノール、エタノールなど)は、イミダゾール化合物およびピラゾール化合物(12)のN-Cbz保護基を除去するために使用できます。n-Bu3SnH/AIBN系などの有機金属試薬は、アミドおよび含窒素ヘテロ芳香族環のN-Cbz保護基を選択的に除去することができ、脂肪族アミンのCbz保護には影響を与えません。これらの方法は、従来のCbz除去法を補完するものであり、本稿では詳細には説明しません。
(12)
まとめると、上記の Cbz 除去法にはそれぞれ長所と短所があり、適切なシナリオがあります。複雑な有機合成反応では、保護基の導入と除去には、特定の反応基質の構造特性に基づいた適切な合成戦略の選択が必要です。
参考文献:
[1] Xu Qiuxia. グルタチオンの化学合成の研究 [D]. Donghua University, 2010.
[2] Pehere, AD; Abell, AD N-Cbz アミノ酸の調製のための改良された大規模手順 [J]. Tetrahedron Lett., 2011, 52, 1493-1494.
[3] Sureshbabu, P.; Azeez, S.; Kandasamy, J., et al. N-Cbz アミドの合成および室温でのアミド基転移反応への応用 [J]. Asian J. Org. Chem., 2022, 11.
[4] Varala, R.; Enugala, R.; Adapa, SR. 分子ヨウ素触媒によるアミンの効率的な N-Cbz 保護 [J]. J. Iran. Chem. Soc., 2007, 4, 370-374.
[5] Zhang, CL; Zhang, DF; Huang, HH; et al. PEG-600 中のアミンの N-Cbz 保護のための簡便なプロトコル [J]. Chinese Chemical Letters, 2012, 23, 789-792.
[6] Cameron, M.; Wilson, RD 対応する CBZ 保護前駆体からの N-ベンジル化第三級アミンの予期せぬ形成 [J]. APPL CATAL A-GEN, 2000, 203, 307-310.
[7] Bajwa, JS ベンジルカルバメートのt-ブチルカルバメートへのワンポット変換[J]. Tetrahedron Lett. 1992, 33, 2955-2956.
[8] Sultane, PR; Mete, TB; Bhat, RG N-ベンジルオキシカルボニル(Cbz)およびベンジルエステル基の脱保護のための便利なプロトコル[J]. Tetrahedron Lett., 2015, 56, 2067-2070.
[9] Vinayagam, V.; Sadhukhan, SK; Kumar, TVH; et al. AlCl3とHFIPの組み合わせによるNベンジルオキシカルボニル(N Cbz)基の脱保護のための穏やかな方法[J]。J. Org. Chem., 2024, 89, 5665-5674.
[10] Papadaki, E.; Georgiadis, D.;
[11] Chen, GH; Pan, P.; Li, ZJ; et al. N-300位に結合したカナマイシンA二量体の容易な合成のためのCbzアミン保護基の選択的脱保護[J]。Tetrahedron, 2009, 65, 5922-5927.
[12] Song, GQ; Huang, XF; Yang, B.; et al. 低炭素アルコールによるN-カルボキシベンジル(Cbz)保護基の容易な除去[J]。Lett. Org. Chem., 2016, 13, 177-180.
[13] Bennasar, ML; Roca, T.; Padullés, A. Cbz保護窒素化合物の化学選択的ラジカル開裂[J]. Org. Lett., 2003, 5, 569-572.